Nove Tópicos Essenciais para Você Explorar a Química é para você ter anotado em sua agenda e levar para todos os lugares. Então, a química é uma ciência central que conecta várias disciplinas e torna nossa compreensão do mundo natural mais fácil. Desde a estrutura dos átomos até as complexas reações que impulsionam os processos biológicos, a química nos ajuda a desvendar os mistérios do universo. Ela não apenas explica a composição e as propriedades das substâncias, mas também nos permite manipular essas substâncias para criar novos materiais e soluções inovadoras para desafios globais.
Neste artigo, exploraremos nove tópicos essenciais dentro da química, cada um destacando sua importância e aplicações práticas. Esses tópicos abrangem desde os fundamentos atômicos e moleculares até as complexidades da química ambiental e orgânica, oferecendo uma visão abrangente de como a química influencia nosso cotidiano e o avanço tecnológico. Ao compreender e aplicar os princípios químicos, podemos desenvolver medicamentos mais eficazes, materiais mais sustentáveis e tecnologias mais eficientes. A química, portanto, não é apenas uma disciplina acadêmica, mas uma força motriz que molda o futuro da ciência e da sociedade. Dessa forma, prepare-se para uma jornada fascinante através dos pilares dessa ciência que transforma nosso mundo.
1. Estrutura Atômica e Tabela Periódica
A estrutura atômica é a base da química, descrevendo como os átomos são formados por prótons, nêutrons e elétrons. Esses componentes fundamentais determinam as propriedades únicas de cada elemento. Os prótons, carregados positivamente, e os nêutrons, sem carga, compõem o núcleo do átomo, enquanto os elétrons, carregados negativamente, orbitam ao seu redor. A interação entre essas partículas define a identidade química do elemento e suas propriedades.

A tabela periódica é uma ferramenta crucial que organiza os elementos de acordo com suas propriedades químicas e físicas. Criada por Dmitri Mendeleev no século XIX e refinada ao longo dos anos, a tabela periódica não apenas classifica os elementos por número atômico, mas também revela padrões periódicos que ajudam a prever o comportamento químico dos elementos. Elementos em grupos ou famílias compartilham características semelhantes, como reatividade e tipos de ligação, devido à configuração de seus elétrons de valência.
Essa organização sistemática permite aos cientistas prever como os elementos irão interagir em reações químicas, facilitando a descoberta de novos materiais e compostos. Por exemplo, ao entender a tendência de reatividade dos metais alcalinos ou a estabilidade dos gases nobres, os químicos podem projetar experimentos mais eficazes e desenvolver novos materiais com propriedades desejadas. Assim, a estrutura atômica e a tabela periódica não são apenas conceitos teóricos, mas ferramentas práticas que impulsionam a inovação na ciência dos materiais, na farmacologia e em inúmeras outras áreas, moldando o futuro da tecnologia e da indústria.
2. Ligações Químicas: Covalentes, Iônicas e Metálicas
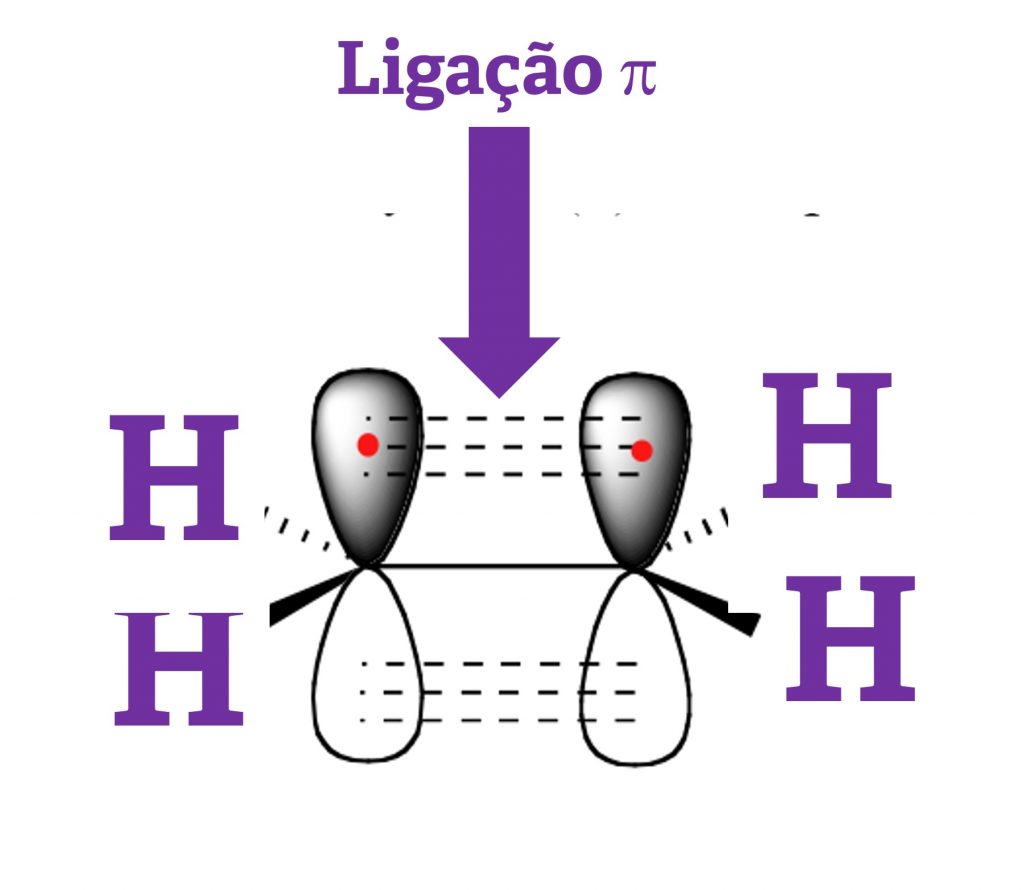
As ligações químicas são forças fundamentais que mantêm os átomos unidos em moléculas e compostos. Assim, elas são importantes na determinação das propriedades e comportamentos das substâncias. A princípio, existem três tipos principais de ligações químicas: covalentes, iônicas e metálicas, cada uma com características e implicações distintas na química.
As ligações covalentes ocorrem sobretudo quando dois átomos compartilham pares de elétrons. Dessa forma, esse compartilhamento permite que cada átomo atinja uma configuração eletrônica estável, semelhante à dos gases nobres. Assim, as ligações covalentes são comuns em compostos orgânicos e moléculas biológicas, como água e DNA, onde a estabilidade e a especificidade das interações são essenciais.
Por outro lado, as ligações iônicas resultam da transferência de elétrons de um átomo para outro, criando íons com cargas opostas que se atraem mutuamente. Então, esse tipo de ligação é típico em sais, como o cloreto de sódio (NaCl), onde a força eletrostática entre os íons positivos e negativos mantém a estrutura cristalina estável.
As ligações metálicas são características dos metais, onde os átomos compartilham um “mar” de elétrons livres que se movem livremente entre eles. Essa delocalização de elétrons confere aos metais suas propriedades únicas, como alta condutividade elétrica e térmica, maleabilidade e ductilidade. Essas propriedades tornam os metais essenciais em diversas aplicações industriais e tecnológicas.
Em resumo, as ligações químicas são fundamentais para a formação e estabilidade das substâncias, influenciando diretamente suas propriedades físicas e químicas e, consequentemente, suas aplicações práticas na vida cotidiana e na indústria.
3. Reações Químicas e Equações Balanceadas

Reações químicas são processos fundamentais na química, nos quais substâncias iniciais, chamadas reagentes, são transformadas em novas substâncias, conhecidas como produtos. Dessa forma, esses processos são onipresentes na natureza e na indústria, ocorrendo em fenômenos tão diversos quanto a digestão dos alimentos, a combustão de combustíveis e a síntese de medicamentos. Além disso, a compreensão dessas transformações é fundamental para o desenvolvimento de novas tecnologias e para a inovação científica.
Por outro lado, a representação das reações químicas por meio de equações balanceadas é essencial para a compreensão e previsão dos resultados dessas transformações. Uma equação química balanceada respeita sobretudo a lei da conservação da massa, que afirma que a massa total dos reagentes deve ser igual à massa total dos produtos. Isso significa que o número de átomos de cada elemento deve ser o mesmo em ambos os lados da equação. Essa representação precisa permite aos químicos prever a quantidade de produtos que uma reação pode gerar a partir de uma determinada quantidade de reagentes, além de otimizar processos industriais e laboratoriais.
A habilidade de balancear equações químicas é, portanto, uma competência fundamental para qualquer químico. Esse processo envolve ajustar os coeficientes dos reagentes e produtos para garantir que a equação atenda à conservação da massa. Dominar essa habilidade é essencial não apenas para a prática laboratorial, mas também para a compreensão teórica dos mecanismos de reação e para a aplicação prática da química em diversas áreas, desde a engenharia química até a biotecnologia.
4. Termodinâmica Química e Energia

A termodinâmica química é uma área essencial da química que se concentra no estudo da energia e suas transformações durante as reações químicas. Este campo abrange conceitos fundamentais como entalpia, entropia e energia livre de Gibbs, que são essenciais para entender e prever o comportamento das reações.
A entalpia refere-se à quantidade de energia absorvida ou liberada durante uma reação, indicando se uma reação é exotérmica ou endotérmica. A entropia, por outro lado, mede a desordem ou aleatoriedade em um sistema, ajudando a compreender a direção natural dos processos. A energia livre de Gibbs combina esses conceitos para determinar a espontaneidade de uma reação. Se a variação da energia livre de Gibbs é negativa, a reação tende a ocorrer espontaneamente sob condições constantes de temperatura e pressão.
A aplicação desses conceitos não se limita à teoria; a termodinâmica química é fundamental para o desenvolvimento de processos industriais eficientes e sustentáveis. Ao entender como a energia é transformada e transferida, os engenheiros químicos podem otimizar reações para minimizar o desperdício de energia e maximizar a produção. Isso é vital na criação de processos que não apenas economizam recursos, mas também reduzem o impacto ambiental, promovendo práticas industriais mais sustentáveis e responsáveis.
5. Cinética Química: Velocidade das Reações

A cinética química é uma área da química que foca no estudo da velocidade das reações e nos fatores que a influenciam. Entre os principais fatores estão a temperatura, a concentração dos reagentes e a presença de catalisadores. Assim, a temperatura afeta a energia cinética das moléculas, aumentando a frequência e a energia das colisões entre elas, o que geralmente acelera as reações. Então, quanto maior a concentração, maior a probabilidade de colisões eficazes entre as partículas.
Catalisadores são substâncias que aumentam a velocidade das reações sem serem consumidas no processo. Eles funcionam ao fornecer um caminho alternativo com menor energia de ativação, facilitando a formação dos produtos. A compreensão da cinética química é vital para otimizar reações tanto em laboratórios quanto em indústrias. Ao ajustar esses fatores, é possível acelerar as reações, tornando os processos mais eficientes e econômicos.
Na indústria, essa otimização é essencial para aumentar a produtividade e reduzir custos. Em laboratórios, entender a cinética permite que os cientistas desenvolvam métodos mais eficazes para sintetizar novos compostos. Assim, a cinética química não só melhora a eficiência dos processos, mas também contribui para o desenvolvimento de tecnologias inovadoras e sustentáveis.
6. Química Orgânica: O Mundo dos Compostos de Carbono
A química orgânica é um ramo fundamental da química que se concentra no estudo dos compostos de carbono, os blocos de construção da vida na Terra. O carbono é único em sua capacidade de formar uma vasta variedade de estruturas complexas, desde hidrocarbonetos simples, como metano e etano, até moléculas biológicas intricadas, por exemplo proteínas e DNA. Essa versatilidade se deve à capacidade do carbono de formar quatro ligações covalentes fortes, permitindo a formação de cadeias e anéis que são a base para estruturas moleculares diversificadas.
A química orgânica é essencial para o desenvolvimento de uma ampla gama de produtos que são vitais para a sociedade moderna. No campo da medicina, ela permite a síntese de medicamentos que tratam inúmeras condições de saúde, desde antibióticos até medicamentos quimioterápicos. Além disso, a química orgânica é importante na produção de plásticos, materiais que revolucionaram a indústria devido à sua durabilidade e versatilidade.
Além disso, a química orgânica é importante na agricultura, através do desenvolvimento de pesticidas e fertilizantes, e na energia, com a criação de combustíveis mais eficientes. Em suma, a química orgânica não só explica a base molecular da vida, mas também impulsiona inovações que melhoram a qualidade de vida e promovem avanços tecnológicos.
7. Química Inorgânica: Além do Carbono

A química inorgânica é um vasto campo da química que abrange o estudo de todos os elementos da tabela periódica, exceto aqueles que formam compostos orgânicos típicos de carbono. Este ramo da química é essencial para a compreensão dos minerais, metais, catalisadores e compostos de coordenação. Além disso, os catalisadores possuem diversas aplicações tecnológicas e industriais.
Os minerais, por exemplo, são estudados para compreender suas propriedades e potencial de extração e uso em materiais de construção e eletrônicos. Os metais, por sua vez, são fundamentais na fabricação de ligas e componentes estruturais devido à sua resistência e condutividade. Além disso, a química inorgânica é vital no desenvolvimento de catalisadores, que aceleram reações químicas sem serem consumidos, sendo essenciais na produção eficiente de produtos químicos em larga escala.
Os compostos de coordenação, que envolvem metais ligadppos a ligantes, têm aplicações em catálise industrial e medicina, incluindo agentes de contraste em ressonância magnética. A química inorgânica também está na vanguarda da nanotecnologia, onde materiais inorgânicos são projetados em escala nanométrica para criar dispositivos com propriedades únicas, como maior força ou reatividade química.
Em resumo, a química inorgânica não só amplia nosso conhecimento sobre os elementos e suas interações, mas também impulsiona inovações tecnológicas que afetam diretamente a indústria e a vida cotidiana.
8. Química Analítica: Medindo o Mundo

A química analítica é uma disciplina essencial que se dedica a identificar e quantificar substâncias em diversas amostras. Utilizando uma variedade de técnicas sofisticadas, ela permite a garantia da qualidade de produtos e no monitoramento ambiental. Entre os métodos analíticos mais comuns estão a espectroscopia, a cromatografia e a eletroforese, cada uma oferecendo soluções específicas para desafios analíticos.]
A espectroscopia baseia-se na interação entre a luz e a matéria para identificar compostos e determinar suas concentrações. Já a cromatografia separa os componentes de uma mistura, permitindo sua análise individual, sendo amplamente utilizada na indústria farmacêutica para garantir a pureza dos medicamentos. A eletroforese, por sua vez, é uma técnica que separa moléculas com base em seu tamanho e carga, sendo fundamental na análise de proteínas e ácidos nucleicos em biotecnologia.
A precisão e a confiabilidade da química analítica são vitais em setores como a farmacêutica, onde a dosagem correta e a pureza dos medicamentos são críticas para a segurança dos pacientes. Na segurança alimentar, essas técnicas garantem que os alimentos estejam livres de contaminantes e aditivos indesejados. Além disso, no monitoramento ambiental, a química analítica ajuda a detectar poluentes e a avaliar a qualidade da água e do ar, contribuindo para a proteção da saúde pública e do meio ambiente.
9. Química Ambiental: Protegendo o Planeta

A química ambiental é uma área crítica da ciência que se concentra em compreender e mitigar os impactos das atividades humanas no meio ambiente. Com o crescimento industrial e urbano, problemas como poluição do ar, da água e do solo, além das mudanças climáticas, tornaram-se desafios globais urgentes. A química ambiental investiga as fontes, reações e efeitos dos poluentes, buscando soluções eficazes para proteger os ecossistemas e a saúde humana.
Um dos enfoques mais promissores dentro da química ambiental é a química verde. Este campo visa o desenvolvimento de processos e produtos sustentáveis que minimizem os danos ecológicos. A química verde promove a utilização de matérias-primas renováveis, a redução do uso de substâncias tóxicas e a melhoria da eficiência energética nos processos químicos. Além disso, incentiva o design de produtos que sejam biodegradáveis ou recicláveis, reduzindo assim o impacto ambiental a longo prazo.
Por meio dessas abordagens, cientistas e engenheiros estão criando tecnologias inovadoras, como catalisadores mais eficientes, métodos de purificação de água, e alternativas aos combustíveis fósseis. A química ambiental e a química verde, portanto, desempenham papéis essenciais na transição para uma economia mais sustentável, ajudando a mitigar os efeitos adversos das atividades humanas e a preservar o planeta para as futuras gerações.
Conclusão
A química é uma ciência dinâmica e multifacetada, com aplicações que permeiam todos os aspectos da vida moderna. Desde a compreensão básica dos átomos até o desenvolvimento de tecnologias inovadoras, a química continua a ser uma força motriz no avanço da ciência e na melhoria da qualidade de vida. Explorar esses nove tópicos oferece uma visão abrangente das contribuições essenciais da química para o nosso mundo.
Este artigo oferece uma visão geral de tópicos essenciais na química. Se precisar de ajustes ou de informações sobre exemplos específicos, por favor, me avise!
Considerações finais
Então, o assunto “Nove Tópicos Essenciais para Você Explorar a Química” foi interessante? Dessa forma, você tem que acessar artigos sobre Profissões da Química. Acesse ai esses artigo só para começar.
- Educação em Química: Preparando a Próxima Geração para Desafios Globais
- A Química no Centro de Tudo: Unindo Física, Biologia e Muito Mais
- Explorando o Universo: O Papel do Químico na NASA
- A Importância da Química Analítica na Farmácia
Mas, caso ainda tenha dúvida, não pense duas vezes junte-se a comunidade do Clube da Química para receber nossas novidades além de tirar suas dúvidas. Assim, conecte-se nas nossas redes sociais:
Facebook e





