Resumidamente, a Primeira Lei da Termodinâmica trata do princípio da conservação de energia existentes nos sistemas termodinâmicos
ΔU = W – Q
Em que Q representa calor, W trabalho e ΔU: variação da energia interna. Então, observa-se que o calor (Q) é a soma de trabalho (W) e da variação da energia interna (ΔU). Por outro lado, a Segunda Lei estuda a transformação do calor em trabalho, mencionada na Primeira Lei.
Como o ocorreu o desenvolvimento da segunda lei da Termodinâmica
Historicamente, a Segunda Lei da Termodinâmica teve seu desenvolvimento pelo francês Nicolas Léonard Sadi Carnot (1796-1832). Assim, é interessa mencionar que nessa época a Primeira Lei da Termodinâmica ainda não eram totalmente conhecida. Dessa forma, a contribuição de Carnot para a Segunda Lei da Termodinâmica pode ser reduzidas a duas conclusões importantes:
- A eficiência de uma máquina (cuja fonte é o calor) depende da natureza do processo cíclico em que ela opera, e não do material que sofre a transformação (substância de trabalho);
- Não existe máquina mais eficiente do que a de Carnot, pois ele descobriu o processo cíclico mais eficiente para converter calor em outras formas de energia.
A Segunda Lei da Termodinâmica teve também as contribuições de Rudolf Clausius (1822-1888), Lord Kelvin (1824-1907) e Max Planck (1858-1947).
O resultado dos trabalhos dos cientista citados anteriormente são dois enunciados que definem a Segunda Lei da Termodinâmica:
- Enunciado de Clausius: o fluxo de calor ocorre espontaneamente do corpo de maior temperatura para o de menor temperatura. O inverso seria uma transformação forçada, que dependeria do fornecimento de energia ao sistema para que ela ocorresse.
- Enunciado de Kelvin-Planck: nenhuma máquina térmica, que funcione em ciclos, pode transformar toda a energia térmica recebida (calor) em energia mecânica (trabalho), ou seja, não existe uma máquina térmica com 100% de rendimento.
Onde a termodinâmica nos leva
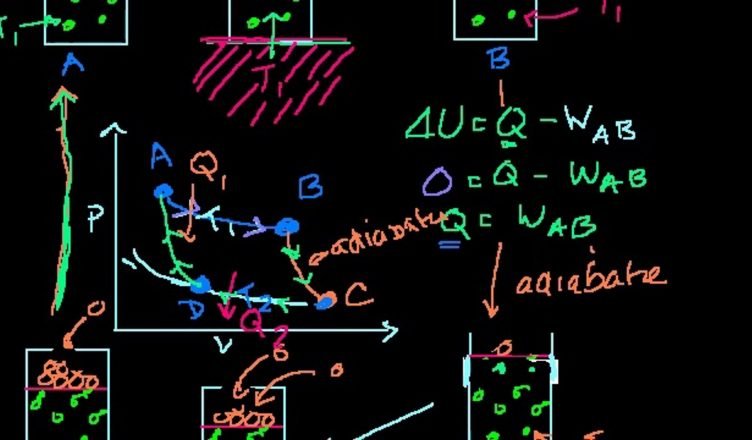
A Segunda Lei da Termodinâmica nos leva a uma conclusão bastante interessante. Os dois enunciados acima nos levar que sempre deverá existir energia térmica sendo rejeitada para a fonte fria (corpo com temperatura menor). Se não existisse uma fonte fria para receber a energia, não seria possível a saída de energia térmica da fonte quente (compor com temperatura maior). Observem o ciclo da Carnot abaixo
Os processos que podem ser observados no vídeo são:
- Expansão isotérmica de A até B, que ocorre quando o gás retira calor da fonte quente;
- Expansão adiabática de B até C, sendo que o gás não troca calor;
- Compressão isotérmica de C até D, pois o gás rejeita calor para a fonte fria;
- Compressão adiabática de D para A, pois não ocorre troca de calor.
Fórmula
Para o cálculo do rendimento de uma máquina de Carnot usamos a seguinte fórmula: R = 1 – T2/T1
Sendo: R o rendimento da máquina de Carnot, T1 a temperatura da fonte quente em Kelvin (K) e T2 a temperatura da fonte fria em Kelvin (K).
Considerações finais
Então, o assunto “Segunda Lei da Termodinâmica” foi interessante? Dessa forma, você tem que acessar mais posts desta vez sobre os elementos químico, por isso convidamos você a acessar a seção da tabela periódica aqui no Clube da Química. Acesse ai.
- Uma Tabela Periódica para o cotidiano
- Onde se aplica a estequiometria no nosso cotidiano?
- Os biocidas fazem parte do nosso cotidiano
- Como é a Química ao nosso redor
- Os utensílios domésticos e a química
Mas, caso ainda tenha dúvida, não pense duas vezes junte-se a comunidade do Clube da Química para receber nossas novidades além de tirar suas dúvidas. Assim, conecte-se nas nossas redes sociais:
Twitter e